Ključna razlika: Emisija je sposobnost tvari da ispušta svjetlo, kada je u interakciji s toplinom. Apsorpcija je suprotnost emisije, gdje energija, svjetlo ili zračenje apsorbiraju elektroni određene tvari.
Emisijski i apsorpcijski spektri su tehnike koje se koriste u kemiji i fizici. Spektroskopija je interakcija zračenja i materije. Koristeći spektroskopiju, znanstvenik može shvatiti sastav određene tvari. To je stvarno korisno, kada se radi s nepoznatim tvarima. Emisijski spektri i apsorpcijski spektri su međusobno različiti, ali još uvijek povezani.

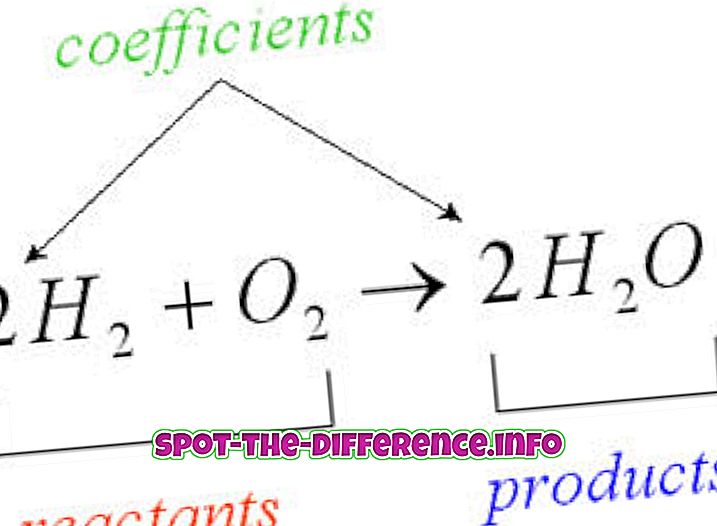
Svaki element ili tvari imaju jedinstvenu razinu emisije ili količinu energije koju zrači; to pomaže znanstvenicima da identificiraju elemente u nepoznatim tvarima. Emisija jednog elementa je zabilježena na spektru emisije ili atomskom spektru. Emitiranje objekta mjeri koliko svjetlosti emitira. Količina emisije objekta varira ovisno o spektroskopskom sastavu objekta i temperaturi. Frekvencije na emisionom spektru zabilježene su u frekvencijama svjetlosti, gdje boja svjetla određuje frekvenciju. Frekvencije se mogu odrediti pomoću formule Ephoton = hv, gdje je 'Ephoton' energija fotona, 'v' je njezina frekvencija, a 'h' je Planckova konstanta. Emisija se može dogoditi u obliku svjetla i zraka, kao što su gama i radio. Spektar je tamna valna duljina s trakama boje na njoj, koja se koristi za određivanje emisije objekta.
Apsorpcija je suprotno od emisije, gdje energija, svjetlo ili zračenje apsorbiraju

Apsorpcija se koristi za određivanje prisutnosti određene tvari u uzorku ili količine predmetne tvari u uzorku. Također se koriste u molekularnoj i atomskoj fizici, astronomskoj spektroskopiji i daljinskom istraživanju. Apsorpcija je primarno određena atomskim i molekularnim sastavom materijala. Oni također mogu ovisiti o temperaturi, elektromagnetskom polju, interakciji između molekula uzorka, kristalnoj strukturi krutina i temperaturi. Da bi se odredila razina apsorpcije tvari, snop zračenja usmjeren je na uzorak i odsutnost svjetlosti koja se reflektira kroz objekt može se koristiti za izračunavanje apsorpcije. Apsorpcijski spektar je obično svijetao, s tamnim trakama koje prolaze kroz njega. Ove tamne trake koriste se za određivanje apsorpcije objekta.
Emisija | Apsorpcijski spektri | |
Opis | Emisija je sposobnost tvari da ispušta svjetlost, kada je u interakciji s toplinom. | Apsorpcija je suprotnost emisije, gdje energija, svjetlo ili zračenje apsorbiraju elektroni određene tvari. |
teme | Kemija i fizika | |
Svrha | Može se koristiti kao dio spektroskopije kako bi se odredio sastav određene tvari. | Može se koristiti kao dio spektroskopije kako bi se odredila razina apsorpcije određenih objekata i njihova sposobnost zadržavanja topline. Također se može koristiti u molekularnoj i atomskoj fizici, astronomskoj spektroskopiji i daljinskom istraživanju. |
vrste | - | Atomski apsorpcijski spektri i molekularni apsorpcijski spektri. |
Utjecaj na molekule | Kada supstanca stupa u interakciju sa svjetlom, neke njezine molekule apsorbiraju toplinu iz svjetla i uzbuđuju se. To uzrokuje da postanu nestabilni i pokušavaju emitirati višak energije da se vrate u normalu. Uzbuđene molekule oslobađaju višak energije u obliku fotona, također poznatih na svjetlosnim česticama. | Kada supstanca stupa u interakciju sa svjetlom, neke njezine molekule apsorbiraju svjetlost ili zračenje. Vrste valne duljine svjetlosti koje se apsorbiraju mogu se mapirati. |
Proizlaziti | Vrsta emitiranih fotona pomaže utvrditi vrstu elemenata od kojih je tvar formirana, budući da svaki element ili tvari imaju jedinstvenu razinu emisije ili količinu energije koju zrači | Vrsta svjetlosnih valnih duljina koje se apsorbiraju pomaže utvrditi koliko je tvari prisutna u uzorku. |
Jednostavno rečeno | Emisijski spektri bilježe valne duljine koje emitiraju materijali, koji su prije bili stimulirani energijom. | Spektri apsorpcije bilježe valne duljine koje je materijal apsorbirao |
Izgleda kao | Tamno obojene, s laganim trakama koje prolaze kroz njega. Ove svjetlosne trake koriste se za određivanje tipova fotona koje emitira objekt. | Svijetle boje, s tamnim trakama koje prolaze kroz njega. Ove tamne trake koriste se za određivanje apsorpcije objekta. |
Jedinice | Frekvencije emisije mogu se odrediti pomoću formule Ephoton = hv, gdje je 'Ephoton' energija fotona, 'v' je njezina frekvencija, a 'h' je Planckova konstanta. | Može se iscrtati u valnoj duljini, frekvenciji ili valnom broju. |