Ključna razlika: ionska veza je kemijska veza između dva različita (tj. Metalnog i nemetalnog) atoma u kojima jedan atom daje elektron drugima. Kovalentna veza je druga jaka kemijska veza. Događa se slični atomi (tj. Dva nemetala). U kovalentnoj vezi dva atoma dolaze zajedno kako bi dijelila elektron, umjesto da atom uzima drugi iz drugog.
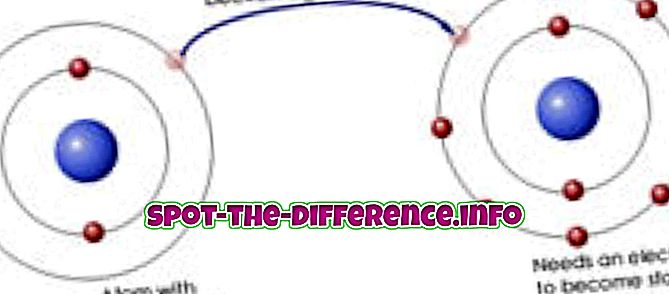
Ionska veza je kemijska veza između dva različita (tj. Metalnog i nemetalnog) atoma u kojima jedan atom daje drugi elektron. Stoga oba atoma postaju ioni jer jedan atom ima jedan elektron manje, dok drugi ima ekstra. Metalni ion koji je izgubio elektron ima pozitivan naboj. Ne-metalni ion koji je dobio elektron ima negativan naboj. Kako se suprotnosti privlače, ovi ioni se onda snažno privlače jedni drugima, tako snažno da postanu povezani.
Ionski spojevi su obično u obliku krutina, tj. Soli. Vrlo su topljivi u vodi i imaju visoku točku taljenja. Kada su u vodi, također imaju visoku električnu vodljivost.

Kovalentno vezanje uključuje mnoge vrste interakcija, uključujući σ-vezanje, π-vezanje, spajanje metala na metal, agostičke interakcije i trocentralne veze s dva elektrona. Kada atom ima svoj elektron u svojoj vanjskoj ljusci i drugi atomi zahtijevaju od elektrona da ispuni svoju vanjsku ljusku, dva atoma neka zajedno dijele elektron. Dakle, oba atoma imaju krajnju vanjsku ljusku, a time i stabilnu elektroničku konfiguraciju.
Kemijske veze su načinjene tako da atom može imati punu vanjsku ljusku, jer puna vanjska ljuska znači stabilnu elektronsku konfiguraciju. U ionskoj vezi, kada metalni atom ima jedan elektron u svojoj vanjskoj ljusci, a ne-metal treba elektron za dovršenje svoje vanjske ljuske, atom metala daje svoj elektron nemetalu. Slično tome, u kovalentnoj vezi podjednako dijele elektron.
Ionska Bond | Kovalentna veza | |
definicija | Kemijska veza između dva različita atoma u kojima atom predaje elektron drugom. | Kovalentna veza je kemijska veza koja uključuje dijeljenje elektrona između dva slična atoma. |
događaj | Metalni i nemetalni | Dva nemetala |
Polaritet | visok | nizak |
Oblik molekule | Nema određenog oblika, rešetkastih struktura | Definirani oblik |
Električna provodljivost | visok | Obično ništa |
Toplinska vodljivost | visok | Obično niska |
Točka taljenja tvari | Razlikuje se, ali je obično viši od kovalentnih spojeva | Mijenja se, ali obično je niži od ionskih spojeva |
Točka vrenja tvari | visok | Mijenja se, ali obično je niži od ionskih spojeva |
Topljivost u vodi | visok | Mijenja se, ali obično je niži od ionskih spojeva |
Stanje tvari na sobnoj temperaturi | Obično čvrsta | Čvrsta, tekuća, plinovita |