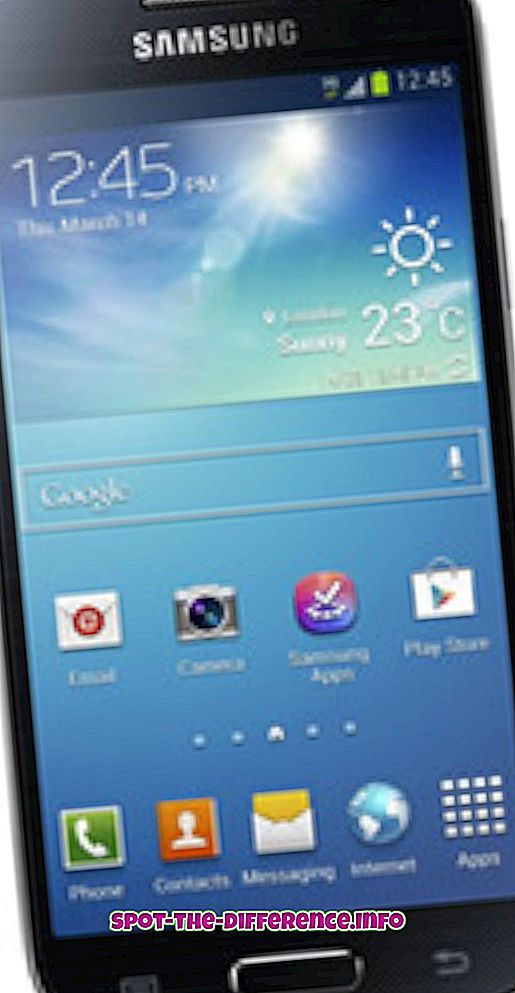
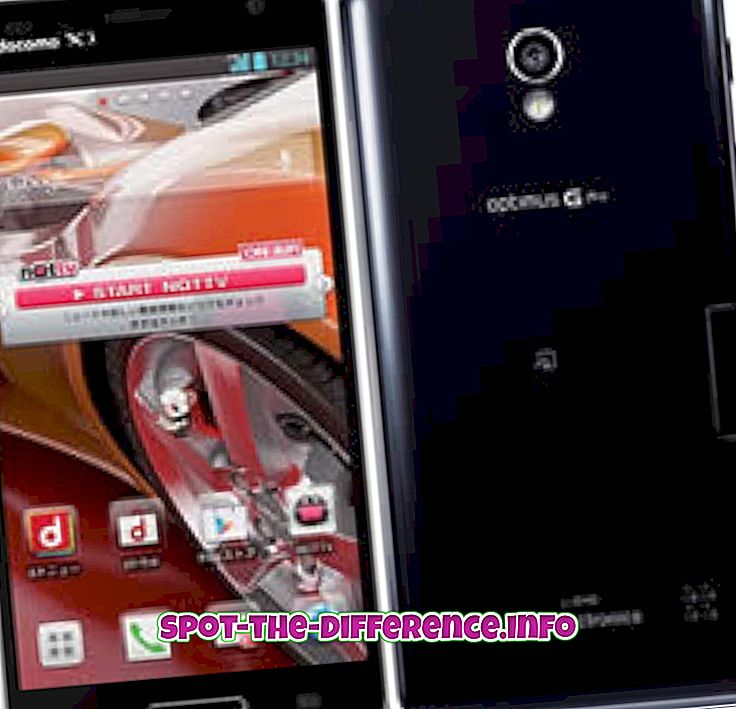
Ključna razlika: Atomi su osnovne jedinice od kojih je sva materija izrađena. Atomi su maleni, u rasponu od 0, 1 do 0, 5 nanometara u širini. Svaki atom bilo kojeg elementa sastoji se od protona, neutrona i elektrona. Atomi različitih elemenata spajaju se kako bi stvorili molekule. To se događa kemijskom reakcijom. Molekula je najmanja količina kemijske tvari koja može postojati.
Element je čista kemijska tvar koja ima jedan ili jedan tip atoma koji se razlikuje po svojem atomskom broju. Atomski broj je izveden iz broja protona prisutnih u jezgri elementa. Ukupno je identificirano 118 elemenata, podijeljenih između metala, metaloida i nemetala. Svaki element ima svoj vlastiti skup svojstava. Većina elemenata dostupna je na Zemlji, dok je nekoliko njih umjetno razvijeno kroz nuklearne reakcije. Element je već u najsitnijem obliku i ne može se dalje podijeliti. Svi elementi se mogu naći u Periodnom sustavu, navedenom po atomskom broju.
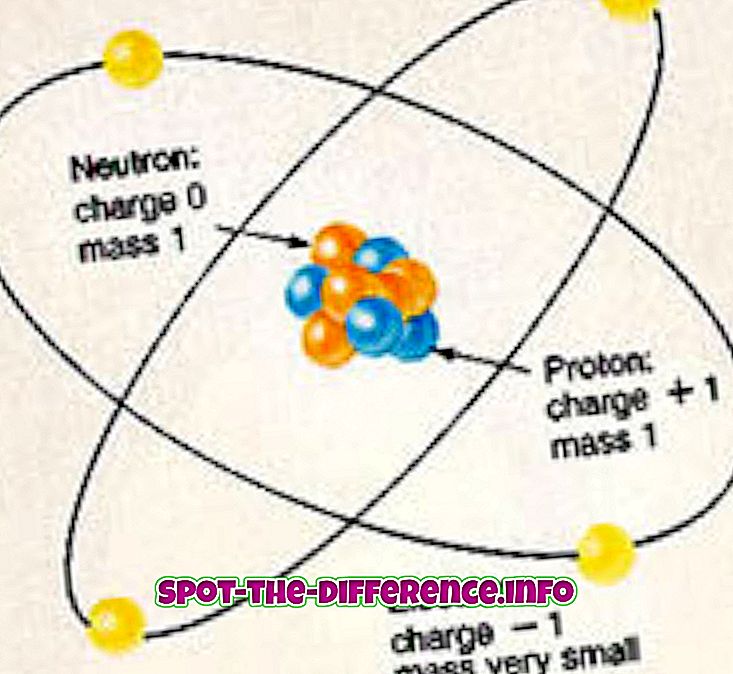
Svaki atom bilo kojeg elementa sastoji se od protona, neutrona i elektrona. Protoni i neutroni čine jezgru atoma i nalaze se u sredini atoma. Jezgra je okružena oblakom elektrona koji su elektromagnetskom silom vezani za jezgru. Elektroni imaju negativan naboj koji ih privlači jezgra, jer protoni u jezgri imaju pozitivan naboj. Neutroni, s druge strane, nemaju punjenje.
Broj protona, neutrona i elektrona u atomu određuje koji je to element. Na primjer: Atom željeza ima 26 protona, 30 neutrona i 26 elektrona. Svaki atom željeza ima takvu konfiguraciju.
Atomi različitih elemenata spajaju se kako bi stvorili molekule. To se događa kemijskom reakcijom. Na primjer: dva atoma vodika i jedan atom kisika kombiniraju molekule vode.

Molekula može imati vrlo različita svojstva od elemenata od kojih je napravljena. Na primjer: voda se ponaša vrlo različito od kisika ili vodika, iako se sastoji od dva atoma vodika i jednog atoma kisika.
Nadalje, atom ne može postojati nezavisno u prirodi bez vezivanja za nešto. Nikada nećemo naći samo jedan atom kisika ili jedan atom ugljika. Uvijek je povezan s nečim, kao što je O2 (kisik) ili CO2 (ugljični dioksid). Kada se veže u molekulu, molekula može postojati neovisno u prirodi, zbog čega uvijek možemo pronaći molekulu kisika, molekulu ugljičnog dioksida, molekulu vode (H2O) itd.
U molekuli, atomi su spojeni u određenom obliku ili obliku. To uglavnom ovisi o broju veza koje atom može napraviti. Atomi formiraju molekule formiranjem kemijskih veza jedna s drugom. Atomi kisika uvijek imaju dvije veze s drugim atomima, ugljikovi atomi uvijek imaju četiri veze s drugim atomima, a atomi dušika uvijek imaju tri veze s drugim atomima. Zbog toga određena vrsta molekula uvijek ima određeni oblik, kao što je peterokutna, šesterokutna, lateralna, bi-lateralna itd.
Molekule uvijek teže grupirati se, njihova formacija ovisi o njihovom stanju. Kao u plinovitom stanju, molekule imaju tendenciju da samo lete okolo. U tekućem stanju, molekule imaju tendenciju da budu labavo grupirane tako da se i dalje mogu kretati. Dok su u čvrstom stanju, molekule su čvrsto spakirane i mogu samo vibrirati.
Molekule su obično zastupljene u molekularnoj formuli. Na primjer: O2, H20, CO2, C6H12O6 (šećer). Molekularna formula je naziv elementa, nakon čega slijedi broj atoma tog elementa u molekuli.