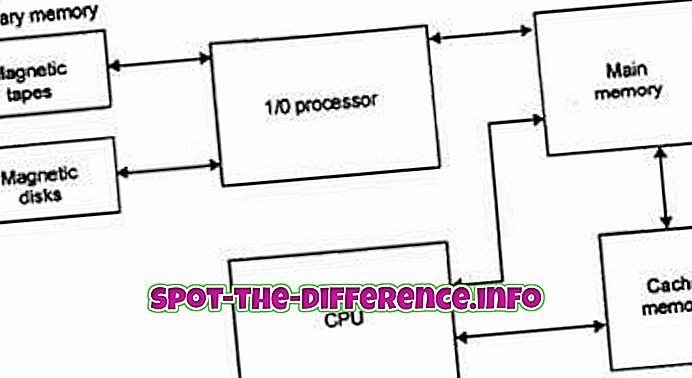
Ključna razlika: Apsorpcija je rasuti fenomen u kojem apsorbat potpuno prodire u tijelo krute tvari ili tekućine kako bi stvorio spoj ili otopinu. S druge strane, adsorpcija je površinska pojava u kojoj se molekule adsorbata koncentriraju samo na površini adsorbenta.
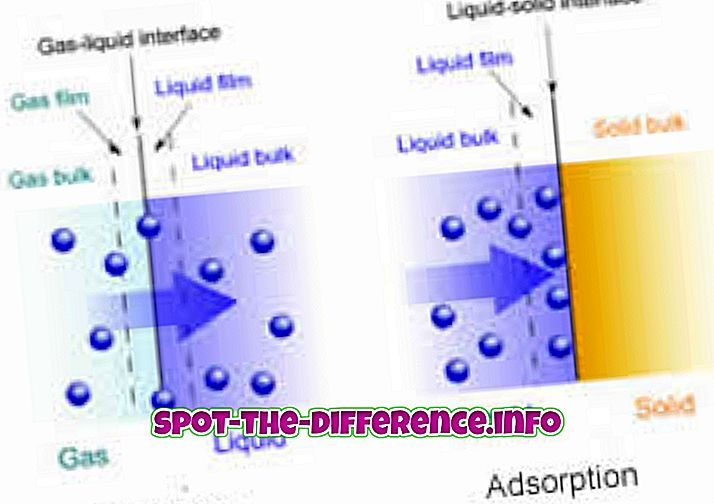
Kemijska reakcija - ugljični dioksid apsorbira otopina kalijevog ugljika
Fizički proces - Zrak se apsorbira u vodi otapanjem

Postoje dva tipa adsorpcijskih načina - kemijski i fizikalni. U kemijskoj adsorpciji molekule i površinu vežu slabe Vander Wallsove sile. S druge strane, u kemijskoj adsorpciji nastaje kemijska veza između molekula i površine.
Stoga je primarna razlika između adsorpcije i apsorpcije ta da je apsorpcija rasuti fenomen, što znači da se događa u cijelom tijelu materijala, dok adsorpcija ostaje površinski fenomen. Adsorpcija je uvijek egzotermna, dok je apsorpcija endotermna. Sorpcija uključuje oba procesa apsorpcije i adsorpcije.
Usporedba adsorpcije i apsorpcije:
Adsorpcija | apsorpcija | |
Defintion | Akumulacija plina ili tekuće otopine na površini krutine ili tekućine | Difuzija tvari u tekućinu ili krutinu da se dobije otopina ili spoj |
Primjer | Inertni plinovi se adsorbiraju na drvenom ugljenu. | Suha spužva upija vodu |
Izmjena topline | Egzotermna s izuzetkom adsorpcije H2 na staklu | cndotcrmni |
Postizanje ravnoteže | Usporedno brže | Usporedno polako |
Koncentracija | Koncentracija na površini adsorbenta je različita od one u masi | Koncentracija ostaje ista u cijelom materijalu |
Stopa pojave | U početku je brz, ali kasnije stopa počinje opadati | Ona se odvija jednakom brzinom |